Перейти к:
Исследование цитокинового профиля в периферической крови и головном мозге у пациентов с фокальной фармакорезистентной эпилепсией
https://doi.org/10.47093/2218-7332.2021.12.4.39-50
Аннотация
Цель исследования. Изучить у пациентов с фармакорезистентной эпилепсией (ФРЭ) маркеры дисфункции гематоэнцефалического барьера (ГЭБ) – содержание VEGF в эндотелиоцитах капилляров мозга, TNF-α в ткани мозга и цитокиновый профиль в сыворотке крови.
Материалы и методы. В исследование включены 30 пациентов с ФРЭ, которым проведена передняя темпоральная блок-резекция. Исследованы гистологические образцы головного мозга для оценки содержания VEGF и TNF-α; определена концентрация цитокинов в сыворотке крови.
Результаты. В группе ФРЭ денситометрическая плотность клеток, экспрессирующих VEGF и содержание TNF-α в эпилептическом очаге, была выше, чем в контрольных группах (p < 0,001; p < 0,05). По сравнению с контролем в сыворотке крови пациентов с ФРЭ концентрация IL-2 (0,98 ± 0,28 против 2,80 ± 0,71 пг/мл; p < 0,001), IL-8 (14,04 ± 1,46 против 26,13 ± 3,80 пг/мл; p < 0,001) и EGF (43,72 ± 5,63 против 83,62 ± 24,06 пг/мл; p < 0,05) была статистически значимо ниже, а содержание TNF-α (33,09 ± 1,23 против 24,85 ± 1,32 пг/мл, p < 0,05), IL-4 (43,73 ± 2,57 против 32,37 ± 5,80 пг/мл, p < 0,05), IL-5 (43,73 ± 2,57 против 32,37 ± 5,80 пг/мл; p < 0,05), IL-7 (16,65 ± 3,07 против 8,13 ± 1,67 пг/мл; p < 0,05), GRO (growth-regulated protein) (3054,0 ± 200,8 против 1367,0 ± 187,3 пг/мл; p < 0,001), VEGF (316,10 ± 55,28 против 95,22 ± 15,78 пг/мл; p < 0,01) статистически значимо выше. Существенных различий по концентрации IL-1β, IL-1RA, IL-10 и IFN-γ между группами ФРЭ и контролем не установлено.
Заключение. Исходя из изученного цитокинового профиля можно заключить, что у пациентов с ФРЭ отсутствует системное воспаление. Установленная гиперэкспрессия VEGF в головном мозге и увеличение концентрации его в крови в сочетании со снижением концентраций EGF в сыворотке крови и повышением GRO, а также провоспалительных факторов свидетельствует о повреждении ГЭБ. Высокое содержание TNF-α непосредственно в эпилептическом очаге свидетельствует о нейровоспалении, и в условиях дисфункции ГЭБ можно обнаружить повышенную концентрацию TNF-α в крови пациентов.
Ключевые слова
Список сокращений:
VEGF – vascular endothelial growth factor, фактор роста эндотелия сосудов
IFN-γ – interferon gamma, интерферон гамма
IL – interleukin, интерлейкин
EGF – epidermal growth factor, эпидермальный фактор роста
GRO – growth-regulated protein / growth-regulated oncogene, белок регулировки роста
TNF-α – tumor necrosis factor alpha, фактор некроза опухоли альфа
ГЭБ – гематоэнцефалический барьер
ИГХ – иммуногистохимическое исследование
ФРЭ – фармакорезистентная эпилепсия
ЦНС – центральная нервная система
Эпилепсия является серьезной проблемой для здравоохранения во всем мире. Доля пациентов с эпилепсией составляет 1% от общего числа всех заболеваний [1]. Несмотря на успехи фармакологии, у более чем 30% пациентов заболевание прогрессирует до формирования лекарственно-устойчивой эпилепсии и нуждается в хирургическом лечении [2]. Развитие резистентности к противоэпилептическим средствам может быть связано с нарушениями проницаемости гематоэнцефалического барьера (ГЭБ).
ГЭБ изменяется при многих патологиях центральной нервной системы (ЦНС), и эти изменения включают активацию молекул адгезии в просвете сосудов, повышенную адгезию и трансмиграцию лейкоцитов, повышенную проницаемость плотных контактов и экстравазацию белков плазмы [3].
Ранее в экспериментальных и клинических работах было установлено, что в очагах длительно протекающей эпилепсии увеличивается проницаемость ГЭБ, а искусственно вызванная дисфункция ГЭБ приводит к появлению эпилептических очагов в ранее здоровом мозге [4][5].
На проницаемость ГЭБ значимое влияние оказывают медиаторы воспаления и цитокины [6]. Так, фактор роста эндотелия сосудов А (VEGF-A – vascular endothelial growth factor A, далее VEGF) является промотором неоваскуляризации и его увеличение приводит к повышению проницаемости сосудов и нарушению целостности ГЭБ из-за дестабилизации плотных контактов [7][8], мобилизации воспалительных клеток к месту повреждения, поддержанию местного воспалительного процесса и индукции синтеза проангиогенных факторов эндотелиальными клетками [8][9]. VEGF секретируется эндотелиальными и другими клетками в ответ на кислородное голодание. Показано, что в неокортексе пациентов с фармакорезистентной мезиальной височной эпилепсией (ФРЭ) увеличивается концентрация белков VEGF-A, VEGF-B и VEGF-C, их специфических рецепторов VEGFR-2 и VEGFR-3, корецепторов киназы NRP-1 и NRP-2 (neuropilin-1 and -2, нейропилин-1 и -2), а также киназы PI3 (phosphoinositide 3-kinases, фосфоинозитид-3-киназы) и Akt (alpha serine/threonine-protein kinase, альфа серин/треонин протеинкиназа) [10]. Это подчеркивает потенциальную роль системы VEGF в патогенезе ФРЭ.
Установлено, что уровень интерлейкина-1 альфа (IL-1α, interleukin 1 alpha) – провоспалительного цитокина – у пациентов с эпилепсией выше, чем в контрольной группе (без эпилепсии) [11], независимо от наличия склероза гиппокампа [12]. Повышенная экспрессия IL-1β обнаружена у пациентов с височной эпилепсией по сравнению с контрольной группой аутопсии [13], наиболее высокий уровень экспрессии отмечен у пациентов со склерозом гиппокампа [14].
В отличие от данных, обнаруженных в ткани мозга, уровень IL-1β в сыворотке пациентов с височной эпилепсией не был повышен по сравнению со здоровым контролем [15]. Вместе с этим сообщалось о снижении соотношения антагониста рецептора интерлейкина-1 (interleukin-1 receptor antagonist, IL-1RA) IL-1RA/IL-1β после приступа, что приводит к усилению влияния IL-1β и может указывать на провоспалительное состояние в головном мозге [16]. Противосудорожный эффект IL-1RA показан на пилокарпиновой мышиной модели и у лиц с тяжелыми формами эпилепсии [17].
Другими медиаторами воспаления, которые могут нарушать работу плотных контактов, являются интерферон гамма (interferon gamma, IFN-γ) и IL-17A, цитокины, продуцируемые Т-хелперами (T-helper) Th17 и Th1, а также другими субпопуляциями лейкоцитов. IFN-γ и IL-17A вовлечены в патогенез заболеваний ЦНС, включая рассеянный склероз, эпилепсию и инсульт [18]. Кроме того, показано, что IFN-γ, IL-17A или зонулин могут быстро увеличивать проницаемость ГЭБ in vitro, модифицируя плотные контакты и лежащий в основе актиновый цитоскелет [19].
Было показано, что фактор некроза опухоли альфа (tumor necrosis factor-alpha, TNF-α) увеличивает среднюю частоту AMPA-зависимых (alpha-amino-3-hydroxy-5-methyl-4-isoxazole, α-амино-3-гидрокси-5-метил-4-изоксазолпропионовая кислота) миниатюрных возбуждающих постсинаптических токов в нейронах гиппокампа и снижает GABAA-опосредованную (γ-aminobutyric acid type A, γ-аминомасляная кислота А рецептор) тормозную силу синапсов. Эти эффекты, вероятно, опосредованы способностью TNF-α активировать рекрутирование рецепторов AMPA, лишенных субъединицы GluR2, на мембранах нейронов, и таким образом, в молекулярной конформации, которая способствует притоку Ca2+ в нейроны и индуцирует эндоцитоз рецепторов GABAA [20][21]. Эти быстрые посттрансляционные эффекты воспалительных цитокинов представляют собой новые пути, с помощью которых воспалительные молекулы, продуцируемые в пораженной ткани, могут влиять на нейротрансмиссию и способствовать повышенной возбудимости и связанной с ней неврологической симптоматике.
При ФРЭ нарушение структуры плотных контактов и, как следствие, дисфункция ГЭБ могут быть обусловлены медиаторами воспаления. Прямое воздействие на эндотелий сосудов головного мозга провоспалительных цитокинов рассматривается как одна из причин судорог, не поддающихся контролю противоэпилептическими препаратами [22].
Цель исследования: изучить у пациентов с ФРЭ маркеры дисфункции ГЭБ: содержание VEGF в эндотелиоцитах капилляров мозга, TNF-α в ткани мозга и цитокиновый профиль в сыворотке крови.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование одобрено этическим Комитетом Российского научно-исследовательского нейрохирургического института им. проф. А.Л. Поленова – филиала НМИЦ им. В.А. Алмазова Санкт-Петербурга (протокол № 0305-2016 от 16.05.2016) и проводилось в соответствии с Хельсинкской декларацией о правах человека. Предоперационное обследование и хирургическое лечение пациентов проводилось в соответствии с Клиническими рекомендации Ассоциации нейрохирургов России 2015 г.1
Все пациенты, поступившие на хирургическое лечение с 03.09.2018 по 06.04.2020 с диагнозом по МКБ-10 «G40.2 Височно-долевая фокальная эпилепсия структурной этиологии с частыми полиморфными приступами, фармакорезистентное течение» (n = 74), проспективно оценены по критериям включения, невключения и исключения.
Критерии включения:
- возраст 18 лет и старше;
- эпилептиформная активность преимущественно в височной доле головного мозга;
- установленная фармакорезистентность заболевания (приступы сохраняются после применения двух одобренных базовых для данной формы эпилепсии антиэпилептических препаратов в максимально переносимых дозах в виде последовательной монотерапии или в комбинации);
- отсутствие первичного патологического субстрата;
- подтверждение диагноза с помощью инвазивного электроэнцефалографического мониторинга;
- подписанное информированное согласие на взятие, транспортировку, хранение и исследование биологических материалов.
Инвазивный электроэнцефалографический мониторинг проводился с использованием комплекса Medtronic NIM-Eclipse™ E4 System (Medtronic plc., США) с фильтром верхних частот 70 Гц при постоянной времени 0,1 с. Электрокортикография регистрировалась восьмиконтактным стрип-электродом, установленным на коре височной доли головного мозга.
Критерии невключения:
- наличие опухолей, сосудистых мальформаций или инфекционных заболеваний головного мозга;
- ишемические заболевания головного мозга;
- аутоиммунные заболевания головного мозга;
- эпилепсия с поражением других отделов головного мозга (лобной, теменной доли);
- острые инфекционные, хронические воспалительные заболевания.
Критерий исключения:
- недостаточное количество гистологического материала для проведения исследований.
Исходно на критерии включения/невключения/исключения оценены 74 пациента. У 6 пациентов обнаружены опухоли, у 3 – сосудистые мальформации, у 3 – инфекционные заболевания головного мозга; у 2 – ишемические, у 1 – аутоиммунные заболевания; еще у 22 диагностирована эпилепсия с поражением других отделов головного мозга (лобной, теменной доли) (рис. 1).

РИС. 1. Потоковая диаграмма включения пациентов в исследование
FIG. 1. Flowchart of patient inclusion in the study
Критериям включения соответствовали 37 пациентов. Всем им проведена передняя темпоральная блок-резекция. Во время операции взяты биоптаты коры и белого вещества височной доли головного мозга для оценки содержания VEGF и TNF-α. У 7 количество биоматериала оказалось недостаточным для этих исследований (исключенные пациенты).
В анализ включены 30 пациентов (группа ФРЭ): 17 мужчин и 13 женщин, медиана возраста 27,5 года [ 25; 32 ], 14 с левосторонним, 16 – с правосторонним поражением.
Фиксацию биоптата осуществляли в забуференном нейтральном формалине 10% HISTOSAFE® («БиоВитрум», Россия), затем изготавливались парафиновые срезы по общепринятой методике толщиной 3–5 мкм.
Все исследования биоптатов и сыворотки крови проводились на базе Лаборатории сравнительной биохимии и клеточных функций Института эволюционной физиологии и биохимии им. И.М. Сеченова Российской академии наук.
Исследование гистологических образцов головного мозга
Морфометрический анализ содержания VEGF в эндотелиоцитах капилляров мозга проводили с помощью иммуногистохимического исследования (ИГХ) по стандартной методике с демаскировкой белков в цитратном буфере при нагревании до 95 °С с использованием антител к VEGF (DAKO, Дания). Для визуализации использовали систему Streptavidin-Peroxidase Polymer, Ultrasensitive и хромоген DAB (Sigma-Aldrich, США), срезы докрашивали гематоксилином Джилла, заключали в синтетическую заливочную среду Bio Mount HM (Bio-Optica, Италия). Оценка результата реакции проводилась путем подсчета денситометрической плотности окрашенных клеток относительно фоновых областей в 10 полях зрения в программе PhotoM 1.212.
В качестве группы сравнения (Контроль 1) использовался аутопсийный материал от 10 пациентов, умерших от соматических заболеваний, таких как острый инфаркт миокарда, поликистоз почек с развитием терминальной почечной недостаточности, язвенная болезнь желудка, осложненная кровотечением, мезентериальный тромбоз, тромбоэмболия легочной артерии, и не имевших в анамнезе неврологических расстройств. Посмертная задержка до вскрытия составляла не более 12 часов.
Материал, не вошедший в ИГХ-исследование, был заморожен и передан для проведения иммуноблоттинга. Из замороженных образцов при низких температурах отбирался фрагмент массой от 0,03 до 0,05 г, который смешивался с лизатным буфером в соотношении 1:10 и с ингибиторами протеаз – Protease Inhibitor Cocktail (Sigma-Aldrich, США) и фосфатаз – PhosSTOP (Sigma-Aldrich, США), добавленными в лизатный буфер непосредственно во время приготовления проб. После этого образцы центрифугировали 15 минут при температуре 4 °C с относительным центробежным ускорением 12 000 g. По окончании центрифугирования отбирали полученный супернатант, смешивали с буферным раствором Лэммли и инкубировали в течение 5 минут при 95 °С. Полученные образцы изучали методом иммуноблоттинга по стандартной методике, определяли уровень белков: TNF-α (1:1000) (Abcam, США) и тубулина (tubulin) 1:1000 (CellSignalling, США). Для получения количественных данных использовалась программа ImageJ3, с помощью которой рассчитывалось отношение TNF-α/tubulin. Данный параметр наиболее корректно отображает реальное содержание искомого белка в образце, так как мы делаем поправку на содержание тубулина, одного из белков «домашнего хозяйства», используемых для контроля общего содержания белка.
В группу сравнения (Контроль 2) включены 6 пациентов 28 [ 30,8; 26,8 ] лет без эпилепсии, прооперированные в отдаленном периоде (6–12 мес.) после черепно-мозговой травмы. Образцы коры и белого вещества височной и лобной долей головного мозга получены во время плановых реконструктивных вмешательств, таких как иссечение спаек в зоне глиомезодермального рубца.
Исследование цитокинов в сыворотке крови
Образцы сыворотки крови для исследования цитокинов брались до операции, в утренние часы, натощак, на фоне отсутствия приступов. Исследование проведено у 20 пациентов, у 10 регистрировались частые припадки и бессудорожный период не был зафиксирован. Мультиплексный анализ содержания цитокинов и хемокинов проводился на аппарате Luminex MagPix (Merсk Millipore, США) с использованием панели Milliplex MAP Human Cytokine/Chemokine 35-Plex Panel. Из 35 параметров панели в анализ включены: EGF (epidermal growth factor, эпидермальный фактор роста), GRO (growth-regulated protein, белок регулировки роста), IFN-γ, IL-1RA, IL-2, IL-4, IL-5, IL-7, VEGF.
Методика исследования проведена по всем стандартам и протоколу, рекомендуемому производителем. Кровь для исследования забирали в пробирки с активатором свертывания, оставляли при комнатной температуре, позволяя крови свернуться, после чего центрифугировали 20 минут при скорости 2700 об./мин. Сыворотку отделяли, аликвотировали в эппендорфах, замораживали и хранили при –20 °С.
Концентрацию IL-1β, IL-8, IL-10 и TNF-α определяли на иммунохемилюминесцентном анализаторе Immulite 1000 с помощью наборов производителя Siemens Healthcare Diagnostics Products Ltd., Великобритания. Согласно прилагаемым инструкциям чувствительность метода для IL-1β составляет 1,5 пг/мл, IL-8 – 5 пг/мл, IL-10 – 1 пг/мл, TNF-α – 1,7 пг/мл.
В группу сравнения (Контроль 3) включены 12 добровольцев, медиана возраста 28 [ 27; 30,8 ] лет, подписавших информированное добровольное согласие. Критериями исключения являлись: неврологические заболевания, острые или хронические воспалительные заболевания в стадии обострения, перенесенная за последний месяц острая респираторная вирусная инфекция, аутоиммунные заболевания или иммунодефицитные состояния, беременность. Биологический материал забирался натощак в утренние часы.
Статистический анализ
Тест на нормальность для всех изученных параметров проводили с помощью критерия Шапиро – Уилка. Количественные показатели, соответствующие нормальному распределению, представлены в виде среднего значения и стандартного отклонения, не соответствующие – в виде медианы и интерквартильного размаха (25–75 процентили). Сравнение количественных данных проводилось с помощью непарного критерия Стьюдента, критерия Манна – Уитни. Различия считались статистически значимыми при p < 0,05. Статистическую обработку данных проводили с помощью пакета программы GraphPad Prism 8 (GraphPad Software, США).
РЕЗУЛЬТАТЫ
Морфометрический анализ содержания VEGF в эндотелиоцитах капилляров мозга
У всех пациентов в группе ФРЭ наблюдалась резко выраженная экспрессия VEGF, локализованного преимущественно в цитоплазме эндотелиоцитов, умеренно выраженный периваскулярный отек и утолщение стенки капилляров (рис. 2). Денситометрическая плотность клеток, экспрессирующих VEGF, в группе ФРЭ составила 0,41 ± 0,01 против 0,19 ± 0,02 в группе Контроль 1 (p < 0,001).
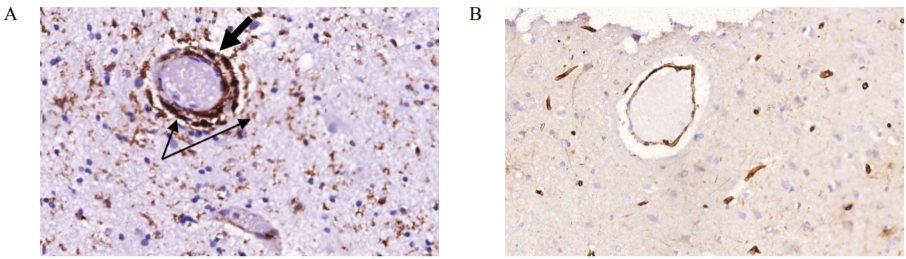
РИС. 2. Морфологические изменения в белом веществе головного мозга
Окраска VEGF антителами, докрашивание гематоксилином, увеличение ×400.
A – умеренно расширенное периваскулярное пространство (толстая стрелка), ярко выраженная положительная реакция на ИГХ-окрашивание VEGF (тонкие стрелки) у женщины 31 года с ФРЭ;
B – отсутствие положительной реакции на окрашивание VEGF у мужчины 39 лет с язвенной болезнью желудка из группы Контроль 1.
Примечание: VEGF – vascular endothelial growth factor, фактор роста эндотелия сосудов; ИГХ – иммуногистохимическое исследование; ФРЭ – фармакорезистентная эпилепсия.
FIG. 2. Morphological changes in the white matter of the brain
VEGF antibody staining, hematoxylin counterstaining, magnification ×400.
А – moderately expanded perivascular space (thick arrow), a pronounced positive reaction to IHC staining of VEGF (thin arrows) in a 31-year-old woman with PhRE;
В – no positive reaction to VEGF staining in 39-year-old man with a gastric ulcer from the Сontrol group 1.
Note: VEGF – vascular endothelial growth factor; IHC – immunohistochemistry; PhRE – pharmacoresistant epilepsy.
Содержание TNF-α в эпилептогенном очаге
Во всех изученных образцах пациентов с ФРЭ выявлено повышенное содержание TNF-α в коре и белом веществе эпилептогенного очага, в коре и в прилежащем белом веществе височной доли головного мозга (рис. 3).
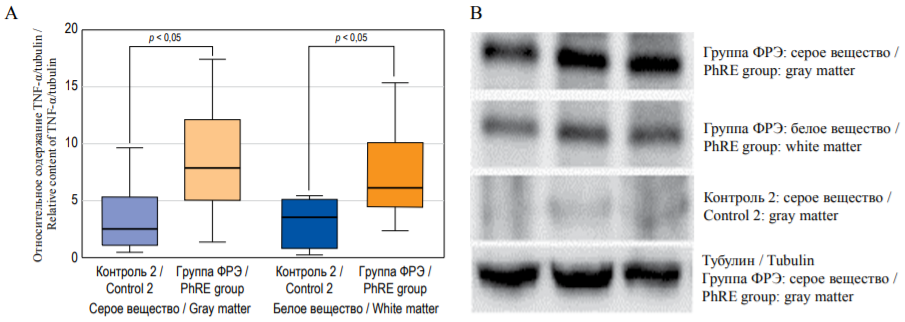
РИС. 3. Относительное содержание TNF-α в сером и белом веществе эпилептогенного очага височной доли
A – содержание в сером и белом веществе;
B – иммуноблоты.
Примечание: ФРЭ – фармакорезистентная эпилепсия.
FIG. 3. Relative content of TNF-α in the gray and white matter of the epileptogenic focus of the temporal lobe
А – contents in the gray and white matter;
B – immunoblots.
Note: PhRE – pharmacoresistant epilepsy.
Содержание цитокинов в сыворотке
В исследуемых образцах сыворотки крови содержание провоспалительного IL-1β и его естественного антагониста IL-1RA существенно не отличалось от их содержания в группе Контроль 3 (табл.). В группе ФРЭ концентрация IL-2, IL-8 и EGF была статистически значимо меньше, чем в группе Контроль 3. При этом содержание TNF-α, IL-4, IL-5, IL-7, GRO, а также VEGF было статистически значимо выше в группе ФРЭ. Содержание противовоспалительных цитокинов IL-10 и IFN-γ значимо не отличалось между группами.
Таблица. Уровень цитокинов и хемокинов в сыворотке крови пациентов с фармакорезистентной эпилепсией по сравнению с группой контроля 3
Table. The level of cytokines and chemokines in the serum of patients with pharmacoresistant epilepsy in comparison with the control group 3
|
Цитокины (пг/мл) / Cytokines, pg/mL |
Группа ФРЭ / PhRE group |
Контроль 3 / Control 3 |
Значение р / р value |
|
IL-1β |
1,26 ± 0,33 |
1,32 ± 0,41 |
n.s. |
|
IL-1RA |
32,99 ± 4,15 |
32,36 ± 6,49 |
n.s. |
|
IL-2 |
0,98 ± 0,28 |
2,80 ± 0,71 |
< 0,001 |
|
IL-4 |
43,73 ± 2,57 |
32,37 ± 5,80 |
< 0,05 |
|
IL-5 |
43,73 ± 2,57 |
32,37 ± 5,80 |
< 0,05 |
|
IL-7 |
16,65 ± 3,07 |
8,13 ± 1,67 |
< 0,05 |
|
IL-8 |
14,04 ± 1,46 |
26,13 ± 3,80 |
< 0,001 |
|
IL-10 |
5,61 ± 0,89 |
4,31 ± 1,15 |
n.s. |
|
TNF-α |
33,09 ± 1,23 |
24,85 ± 1,32 |
< 0,05 |
|
VEGF |
316,10 ± 55,28 |
95,22 ± 15,78 |
< 0,01 |
|
GRO |
3054,0 ± 200,8 |
1367,0 ± 187,3 |
< 0,001 |
|
EGF |
43,72 ± 5,63 |
83,62 ± 24,06 |
< 0,05 |
|
IFN-γ |
13,45 ± 2,05 |
14,17 ± 2,20 |
n.s. |
Примечание: ФРЭ – фармакорезистентная эпилепсия; n.s. – not significant, не значимо.
Note: PhRE – pharmacoresistant epilepsy; n.s. – not significant.
ОБСУЖДЕНИЕ
У наших пациентов из группы ФРЭ была выявлена высокая концентрация VEGF в сыворотке крови, что в дальнейшем может помочь в разработке диагностических тестов по предупреждению развития терапевтической резистентности. Также этот показатель может служить в клинике одним из маркеров нарушения проницаемости ГЭБ [23]. На фоне выявленного нами высокого содержания циркулирующего белка VEGF в плазме крови, индуцирующего эндотелиальную гиперпроницаемость прямым действием на эндотелиальные клетки, высокая экспрессия рецепторов VEGF непосредственно эндотелиоцитами капилляров в головном мозге свидетельствует о том, что эти клетки не получают достаточного количества кислорода в ответ на кислородное голодание [24].
VEGF является потенциальным митогеном для эндотелиальных клеток кровеносных и лимфатических сосудов. Известно, что транскрипция его матричной РНК индуцируется такими цитокинами, как PDGF (platelet-derived growth factor), EGF, TNF-α, TGF-β1 (transforming growth factor beta 1, трансформирующий фактор роста бета 1), IL-1β [25]. В норме VEGF содержится в тканях в незначительном количестве, его экспрессия оказывает сильное влияние на проницаемость сосудов, является мощным ангиогенным белком и принимает участие в процессах неоваскуляризации в патологических ситуациях [26]. Экспрессированный VEGF также способствует мобилизации воспалительных клеток в место повреждения, поддерживая местный воспалительный процесс [9]. Из полученных нами результатов видно, что повышенные уровни белка VEGF обнаруживаются в микрососудах головного мозга при ФРЭ и, скорее всего, могут влиять на основные структурные компоненты плотных контактов. Этот факт в совокупности с выявленным проникновением в кровоток провоспалительных белков, вероятно, свидетельствует о повреждении ГЭБ.
Повышенная концентрация VEGF может служить в клинике одним из маркеров нарушения проницаемости ГЭБ [23]. На фоне выявленного нами высокого содержания циркулирующего белка VEGF в плазме крови, индуцирующего эндотелиальную гиперпроницаемость прямым действием на эндотелиальные клетки, высокая экспрессия рецепторов VEGF непосредственно эндотелиоцитами капилляров в головном мозге свидетельствует о том, что эти клетки не получают достаточного количества кислорода в ответ на кислородное голодание [24].
Хемокин GRO имеет структурное и функциональное сходство с IL-8 и участвует как в воспалении, так и в процессах регулировки роста. По имеющимся литературным данным концентрация GRO может повышаться также при онкологических заболеваниях, в частности при раке яичника или при эссенциальной тромбоцитемии, где повышение провоспалительных цитокинов отражает состояние опухолевого микроокружения и является предиктором неблагоприятного исхода [27, 28]. В контексте эпилепсии данный хемокин изучен недостаточно [29]. В нашем исследовании уровень GRO был статистически значимо выше в группе ФРЭ, что отражает активность воспалительного процесса при наличии эпилепсии и может использоваться в качестве маркера повреждения ГЭБ.
Известно, что под действием цитокинов может нарушаться целостность ГЭБ, а также активироваться и поддерживаться нейровоспаление [30]. Воспаление может быть вовлечено как в возникновение эпилепсии, так и в формирование фармакорезистентности. Нами было установлено, что в исследуемых образцах плазмы крови содержание провоспалительного IL-1β и его естественного антагониста антиконвульсанта IL-1RA существенно не отличалось от содержания их в группе пациентов без эпилепсии, что свидетельствует об отсутствии системного воспаления у пациентов с ФРЭ. Однако в исследовании I.F. Uludag и соавт. установлено снижение IL-1RA/IL-1β [16]. Различия между данными нашего исследования и исследований других авторов могут быть обусловлены временем забора крови: в нашем исследовании забор крови производился в период отсутствия припадков, в исследовании I.F. Uludag и соавт. [16] – после приступа.
Нами зарегистрировано снижение уровня IL-2, важнейшего иммунорегуляторного цитокина, который экспрессируется как клетками иммунной системы, так и клетками головного мозга. Известно, что IL-2 способствует регенерации нейронов после их повреждения, а также стимулирует пролиферацию и дифференцировку олигодендроглиоцитов, его недостаточность в крови пациентов с ФРЭ может быть одним из факторов снижения биодоступности терапевтических препаратов, зависящей от функции ГЭБ [22].
При отсутствии в исследуемой группе с ФРЭ сопутствующих острых инфекционных или хронических заболеваний причиной повышения содержания в крови провоспалительных цитокинов может быть повреждение ГЭБ. Свойства ГЭБ регулируются астроцитами, секретирующими хемокины, такие как EGF, TGF-β и VEGF, которые действуют на эндотелиальные клетки, чтобы либо способствовать образованию плотных контактов, либо регулировать проницаемость ГЭБ [24][31]. VEGF индуцирует эндотелиальную гиперпроницаемость прямым действием на эндотелиальные клетки. Наблюдаемое у наших пациентов с ФРЭ меньшее содержание по сравнению с контролем EGF, отвечающего за рост и деление эндотелиальных клеток, в совокупности с существенно более высоким уровнем VEGF может свидетельствовать о нарушении проницаемости ГЭБ.
Циркуляция в кровотоке таких цитокинов, как TNF-α, IL-1, IL-8, говорит обычно об острой фазе ответа организма на воспаление, которое очень тонко регулируется цитокинами, проявляющими как провоспалительные свойства (IFN-γ), так и действующими как отрицательные регуляторы, ингибируя воспаление (IL-10) [6]. Наши результаты демонстрируют нормальный уровень противовоспалительного IL-10, при этом отмечается повышенное содержание TNF-α и сниженное IL-2 по сравнению с контролем.
Выявленное нами увеличение уровня IL-4, ответственного в организме за уравновешивание возникающего нейровоспаления, может говорить об ответе на появление TNF-α в крови и замедлении синтеза цитокинов первичного ответа. Сниженное содержание стимулятора аниогенеза IL-8 в сыворотке может косвенно указывать на его функциональный дефицит [6], развившийся вследствие хронизации эпилептического процесса.
Обнаруженное нами у пациентов с ФРЭ увеличение в системной циркуляции содержания провоспалительных TNF-α, IL-7 с компенсаторным увеличением концентрации противовоспалительного IL-4, вероятно, отражает реакцию клеток врожденного иммунитета и эндотелия, ассоциированную с повреждением тканей головного мозга [12].
Повышенное содержание TNF-α, одного из основных регуляторов нейровоспаления, в биоптатах коры и белого вещества эпилептогенного очага височных долей по сравнению с пациентами без эпилепсии может свидетельствовать как об активации иммунных клеток в мозге больных ФРЭ, так и о проникновении этого цитокина через ГЭБ. Присутствие TNF-α непосредственно в нервной ткани может говорить об имеющемся нейровоспалении, а попадание этого цитокина в кровоток может быть одним из свидетельств нарушения проницаемости ГЭБ.
Повреждение эндотелия может зависеть от выявленного нами сниженного уровня IL-8. Его снижение может способствовать повышению адгезии нейтрофилов к эндотелиальным клеткам, уже активированным провоспалительными цитокинами, выделяемыми клетками мозга. Таким образом, повышенное образование провоспалительных цитокинов в нервной ткани способствует локальному повышению проницаемости ГЭБ.
Сниженные концентрации EGF относительно контроля говорят о нарушении стимуляции роста и дальнейшего деления эндотелиальных клеток. На фоне выявленного нами высокого содержания циркулирующего белка VEGF в плазме крови, индуцирующего эндотелиальную гиперпроницаемость прямым действием на эндотелиальные клетки, высокая экспрессия рецепторов VEGF эндотелиоцитами непосредственно в микрососудах головного мозга свидетельствует о том, что эти клетки не получают достаточного количества кислорода. Некоторые авторы описали, что проницаемость ГЭБ является одним из факторов, определяющих биодоступность терапевтических препаратов и устойчивость к различным антиэпилептическим препаратам, которые актуальны для пациентов с лекарственной устойчивостью [32].
К ограничениям исследования следует отнести использование аутопсийного гистологического материала в группе контроля с максимальным временем холодовой ишемии до 12 часов.
Дальнейшие исследования в этой области могут служить предпосылкой выявления новой терапевтической мишени в лечении пациентов с ФРЭ, в частности препаратов, нивелирующих эффекты VEGF, нормализующих баланс про- и противовоспалительных цитокинов, а также проницаемость ГЭБ.
ЗАКЛЮЧЕНИЕ
Исходя из изученного цитокинового профиля можно заключить, что у пациентов с ФРЭ отсутствует системное воспаление. Установленная гиперэкспрессия VEGF в головном мозге и увеличение концентрации его в крови в сочетании со снижением в сыворотке крови концентрации EGF и повышением GRO, а также провоспалительных факторов свидетельствует о повреждении ГЭБ. Высокое содержание TNF-α непосредственно в эпилептическом очаге свидетельствует о нейровоспалении, и в условиях дисфункции ГЭБ можно обнаружить повышенную концентрацию TNF-α в крови пациентов.
ВКЛАД АВТОРОВ
Д.А. Ситовская, А.В. Литовченко, Е.Н. Скитева разработали концепцию и дизайн исследования, осуществляли сбор и обработку материала, статистическую обработку данных и написали черновик рукописи. Е.Д. Бажанова и Ю.М. Забродская принимали участие в сборе и обработке материала, редактировании текста. Все авторы утвердили окончательную версию статьи.
AUTHOR CONTRIBUTION
Research concept and design, collection and processing of material, statistical data processing, text writing – Daria A. Sitovskaia, Anastasia V. Litovchenko, Ekaterina N. Skiteva. Collection and processing of material, text editing – Elena D. Bazhanova, Yulia M. Zabrodskaia. All authors approved the final version of the publication.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Исследование цитокинов выполнено в рамках гранта РФФИ № 20-015-00127 и на оборудовании ЦКП ИЭФБ РАН. Иммуногистохимическое исследование проводилось в рамках Госзадания №121031000359-3 «Разработка новых подходов в диагностике медиобазальной фармакорезистентной эпилепсии на основе гистопротеомики эпилептических очагов».
Conflict of interests. The authors declare that there is no conflict of interests.
Financial support. The study of citokines was carried out within the framework of the RFBR grant № 20-015-00127 and on the equipment of the CCU of the IEFB RAS. Immunohistochemical study was performed within the framework State task No. 121031000359-3 "Development of new approaches in the diagnosis of mediobasal pharmacoresistant epilepsy based on histoproteomics of epileptic foci".
1. https://www.ruans.org/Text/Guidelines/epilepsy.pdf
2. http://www.t_lambda.chat.ru/download.html
3. https://imagej.nih.gov/ij/
Список литературы
1. Sheng J., Liu S., Qin H., et al. Drug-Resistant epilepsy and surgery. Curr Neuropharmacol. 2018; 16(1): 17–28. https://doi.org/10.2174/1570159X15666170504123316. PMID: 28474565.
2. Sone D. Making the Invisible Visible: Advanced Neuroimaging Techniques in Focal Epilepsy. Front Neurosci. 2021 Jul 27; 15: 699176. https://doi.org/10.3389/fnins.2021.699176. PMID: 34385902.
3. Abbott N.J., Friedman A. Overview and introduction: the bloodbrain barrier in health and disease. Epilepsia. 2012 Nov; 53 Suppl 6(0 6): 1–6. https://doi.org/10.1111/j.1528-1167.2012.03696.x. PMID: 23134489.
4. Friedman A., Heinemann U. Role of blood-brain barrier dysfunction in epileptogenesis. In: Noebels J.L., Avoli M., Rogawski M.A., Olsen R.W., Delgado-Escueta A.V., editors. Jasper’s Basic Mechanisms of the epilepsies. 4th ed. Bethesda (MD): National Center for Biotechnology Information (US); 2012. PMID: 22787606.
5. Baruah J., Vasudevan A., Köhling R. Vascular Integrity and Signaling Determining Brain Development, Network Excitability, and Epileptogenesis. Front Physiol. 2020 Jan 22;10:1583. https://doi.org/10.3389/fphys.2019.01583. PMID: 32038280.
6. Commins S.P., Borish L., Steinke J.W. Immunologic messenger molecules: cytokines, interferons, and chemokines. J Allergy Clin Immunol. 2010 Feb; 125(2 Suppl 2): S53–72. https://doi.org/10.1016/j.jaci.2009.07.008. Epub 2009 Nov 24. PMID: 19932918.
7. Geiseler S.J., Morland C. The Janus face of VEGF in stroke. Int J Mol Sci. 2018 May 4; 19(5): 1362. https://doi.org/10.3390/ijms19051362. PMID: 29734653.
8. Sweeney M.D., Zhao Z., Montagne A., et al. Blood-brain barrier: from physiology to disease and back. Physiol Rev. 2019 Jan 1; 99(1): 21–78. https://doi.org/10.1152/physrev.00050.2017. PMID: 30280653.
9. Ureña-Guerrero M.E., Castañeda-Cabral J.L., Rivera-Cervantes MC, et al. Neuroprotective and neurorestorative effects of EPO and VEGF: perspectives for new therapeutic approaches to neurological diseases. Curr Pharm Des. 2020; 26(12): 1263–1276. https://doi.org/10.2174/1381612826666200114104342. PMID:31942853.
10. Castañeda-Cabral J.L., Beas-Zárate C., Rocha-Arrieta L.L., et al. Increased protein expression of VEGF-A, VEGF-B, VEGF-C and their receptors in the temporal neocortex of pharmacoresistant temporal lobe epilepsy patients. J Neuroimmunol. 2019 Mar 15; 328: 68–72. https://doi.org/10.1016/j.jneuroim.2018.12.007. Epub 2018 Dec 21. PMID: 30597392.
11. Kan A.A., de Jager W., de Wit M., et al. Protein expression profiling of inflammatory mediators in human temporal lobe epilepsy reveals co-activation of multiple chemokines and cytokines. J Neuroinflammation. 2012 Aug 30; 9: 207. https://doi.org/10.1186/1742-2094-9-207. PMID: 22935090.
12. Aalbers M.W., Rijkers K., Majoie H.J., et al. The influence of neuropathology on brain inflammation in human and experimental temporal lobe epilepsy. J Neuroimmunol. 2014 Jun 15; 271(1–2): 36–42. https://doi.org/10.1016/j.jneuroim.2014.03.016. Epub 2014 Mar 29. PMID: 24746448.
13. Fiala M., Avagyan H., Merino J.J., et al. Chemotactic and mitogenic stimuli of neuronal apoptosis in patients with medically intractable temporal lobe epilepsy. Pathophysiology. 2013 Feb; 20(1): 59–69. https://doi.org/10.1016/j.pathophys.2012.02.003. Epub 2012 Mar 22. PMID: 22444245.
14. Omran A., Peng J., Zhang C., et al. Interleukin-1β and microRNA-146a in an immature rat model and children with mesial temporal lobe epilepsy. Epilepsia. 2012 Jul; 53(7): 1215–1224. https://doi.org/10.1111/j.1528-1167.2012.03540.x. Epub 2012 Jun 18. PMID: 22708826.
15. Nowak M., Bauer S., Haag A., et al. Interictal alterations of cytokines and leukocytes in patients with active epilepsy. Brain Behav Immun. 2011 Mar; 25(3): 423–428. https://doi.org/10.1016/j.bbi.2010.10.022. Epub 2010 Oct 25. PMID: 20977934.
16. Uludag I.F., Bilgin S., Zorlu Y., et al. Interleukin-6, interleukin-1 beta and interleukin-1 receptor antagonist levels in epileptic seizures. Seizure. 2013 Jul; 22(6): 457–461. https://doi.org/10.1016/j.seizure.2013.03.004. Epub 2013 Apr 6. PMID: 23566695.
17. Curia G., Longo D., Biagini G., et al. The pilocarpine model of temporal lobe epilepsy. J Neurosci Methods. 2008 Jul 30; 172(2): 143–157. https://doi.org/10.1016/j.jneumeth.2008.04.019. Epub 2008 Apr 26. PMID: 18550176.
18. Gao F., Gao Y., Zhang S.J., et al. Alteration of plasma cytokines in patients with active epilepsy. Acta Neurol Scand. 2017 Jun; 135(6): 663–669. https://doi.org/10.1111/ane.12665. Epub 2016 Sep 4. PMID: 27593211.
19. Rahman M.T., Ghosh C., Hossain M., et al. IFN-γ, IL-17A, or zonulin rapidly increase the permeability of the blood-brain and small intestinal epithelial barriers: relevance for neuroinflammatory diseases. Biochem Biophys Res Commun. 2018 Dec 9; 507(1–4): 274–279. https://doi.org/10.1016/j.bbrc.2018.11.021. Epub 2018 Nov 16. PMID: 30449598.
20. Beattie E.C., Stellwagen D., Morishita W., et al. Control of synaptic strength by glial TNFalpha. Science. 2002 Mar 22; 295(5563): 2282–2285. https://doi.org/10.1126/science.1067859. PMID: 11910117.
21. Stellwagen D., Beattie E.C., Seo J.Y., Malenka R.C. Differential regulation of AMPA receptor and GABA receptor trafficking by tumor necrosis factor-alpha. J Neurosci. 2005 Mar 23; 25(12): 3219–3228. https://doi.org/10.1523/JNEUROSCI.4486-04.2005. Erratum in: J Neurosci. 2005 Jun 1; 25(22): 1 p following 5454. PMID: 15788779.
22. Bazhanova E.D., Kozlov A.A., Litovchenko A.V. Mechanisms of drug resistance in the pathogenesis of epilepsy: role of neuroinflammation. A literature review. Brain Sci. 2021 May 19; 11(5): 663. https://doi.org/10.3390/brainsci11050663. PMID: 34069567.
23. Matkar P.N., Ariyagunarajah R., Leong-Poi H., Singh K.K. Friends turned foes: angiogenic growth factors beyond angiogenesis. Biomolecules. 2017 Oct 2; 7(4): 74. https://doi.org/10.3390/biom7040074. PMID: 28974056.
24. Sladojevic N., Stamatovic S.M., Johnson A.M., et al. Claudin-1-dependent destabilization of the blood-brain barrier in chronic stroke. J Neurosci. 2019 Jan 23; 39(4): 743–757. https://doi.org/10.1523/JNEUROSCI.1432-18.2018. Epub 2018 Nov 30. PMID: 30504279.
25. Zhu H., Zhang Y., Zhong Y., et al. Inflammation-mediated angiogenesis in ischemic stroke. Front Cell Neurosci. 2021 Apr 21; 15: 652647. https://doi.org/10.3389/fncel.2021.652647. PMID: 33967696.
26. Mühleder S., Fernández-Chacón M., Garcia-Gonzalez I., Benedito R. Endothelial sprouting, proliferation, or senescence: tipping the balance from physiology to pathology. Cell Mol Life Sci. 2021 Feb; 78(4): 1329–1354. https://doi.org/10.1007/s00018-020-03664-y. Epub 2020 Oct 19. PMID: 33078209.
27. Son D.S., Parl A.K., Rice V.M., Khabele D. Keratinocyte chemoattractant (KC)/human growth-regulated oncogene (GRO) chemokines and pro-inflammatory chemokine networks in mouse and human ovarian epithelial cancer cells. Cancer Biol Ther. 2007 Aug; 6(8): 1302–1312. https://doi.org/10.4161/cbt.6.8.4506. Epub 2007 May 26. PMID: 17712227.
28. Øbro N.F., Grinfeld J., Belmonte M., et al. Longitudinal cytokine profiling identifies GRO-α and EGF as potential biomarkers of disease progression in essential thrombocythemia. Hemasphere. 2020 May 21; 4(3): e371. https://doi.org/10.1097/HS9.0000000000000371. PMID: 32647796.
29. Nii T., Yumoto H., Hirota K., Miyake Y. Anti-inflammatory effects of olanexidine gluconate on oral epithelial cells. BMC Oral Health. 2019 Nov 8; 19(1): 239. https://doi.org/10.1186/s12903-019-0932-0. PMID: 31703580.
30. Griffith J.W., Sokol C.L., Luster A.D. Chemokines and chemokine receptors: positioning cells for host defense and immunity. Annu Rev Immunol. 2014; 32: 659–702. https://doi.org/10.1146/annurev-immunol-032713-120145. PMID: 24655300.
31. Abbott N.J., Patabendige A.A., Dolman D.E., et al. Structure and function of the blood-brain barrier. Neurobiol Dis. 2010 Jan; 37(1): 13–25. https://doi.org/10.1016/j.nbd.2009.07.030. Epub 2009 Aug 5. PMID: 19664713.
32. Pérez-Pérez D., Frías-Soria C.L., Rocha L. Drug-resistant epilepsy: From multiple hypotheses to an integral explanation using preclinical resources. Epilepsy Behav. 2021 Aug; 121(Pt B): 106430. https://doi.org/10.1016/j.yebeh.2019.07.031. Epub 2019 Aug 2. PMID: 31378558.
Об авторах
Д. А. СитовскаяРоссия
врач-патологоанатом, научный сотрудник научно-исследовательской
лаборатории патоморфологии нервной системы; ассистент кафедры патологической анатомии
Tel.: +7 (981) 761-31-97
ул. Маяковского, д. 12, Санкт-Петербург, 191014, Россия
ул. Литовская, д. 2, Санкт-Петербург, 194100, Россия
А. В. Литовченко
Россия
аспирант лаборатории сравнительной биохимии и клеточных функций
пр. Тореза, д. 44, Санкт-Петербург, 194223, Россия
Е. Д. Бажанова
Россия
д-р мед. наук, ведущий научный сотрудник лаборатории сравнительной биохимии и клеточных функций; заведующая лабораторией морфологии и электронной микроскопии; старший научный сотрудник кафедры биохимии
пр. Тореза, д. 44, Санкт-Петербург, 194223, Россия
ул. Бехтерева, д. 1, Санкт-Петербург, 192019, Россия
ул. Татищева, д. 20а, Астрахань, 414000, Россия
Е. Н. Скитева
Россия
младший научный сотрудник научно-исследовательской лаборатории патоморфологии нервной системы
ул. Маяковского, д. 12, Санкт-Петербург, 191014, Россия
Ю. М. Забродская
Россия
д-р мед. наук, заведующая научно-исследовательской лабораторией патоморфологии нервной системы; ведущий научный сотрудник лаборатории морфологии и электронной микроскопии; доцент кафедры патологической анатомии
ул. Маяковского, д. 12, Санкт-Петербург, 191014, Россия
ул. Бехтерева, д. 1, Санкт-Петербург, 192019, Россия
ул. Академика Лебедева, д. 6, Санкт-Петербург, 194044, Россия
Дополнительные файлы

|
1. STROBE Statement— Чек-лист по исследованию .pdf | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Скачать
(169KB)
|
Метаданные ▾ | |