Перейти к:
Сравнение безманжетного измерения артериального давления с помощью монитора электрокардиограммы с функцией фотоплетизмографии с измерением по методу Короткова: пилотное исследование
https://doi.org/10.47093/2218-7332.2021.12.1.39-49
Аннотация
Цель: оценить корреляцию между результатами измерений артериального давления с использованием обычного сфигмоманометра с манжетой и результатами портативного монитора электрокардиограммы с функцией фотоплетизмографии.
Материал и методы: В исследование были включены 50 пациентов в возрасте от 33 до 85 лет (средний возраст 63 года), страдающих артериальной гипертензией. Каждому участнику исследования выполнялось 3 измерения артериального давления с использованием сфигмоманометра с подходящей по размеру манжетой и высчитывалось среднее значение. Затем не более чем через одну минуту после последнего измерения проводилась 3-х минутная запись электрокардиограммы и фотоплетизмограммы с помощью одноканального монитора электрокардиограммы CardioQVARK®, выполненного в виде чехла для смартфона. Значения систолического и диастолического артериального давления рассчитывались с использованием комбинации кардиосигнала и фотоплетизмограммы с помощью специально разработанного алгоритма, основанного на машинном обучении. В дальнейшем данные сравнивались со значениями, полученными при использовании сфигмоманометра.
Результаты: Всего было обследовано 55 пациентов и было получено 100 измерений артериального давления от 50 пациентов (5 пациентов по разным причинам были исключены из исследования). По данным анализа Бланда-Альтмана стандартное отклонение для систолического артериального давления составило 4,19, стандартная ошибка среднего – 0,59, Bias= - 0,428. Для диастолического артериального давления стандартное отклонение составило 3,59, стандартная ошибка среднего – 0,51, Bias= - 0,38. Корреляция между показателями сфигмоманометра и монитора CardioQVARK® была равна 0,98(p=0,02) для систолического и 0,88 (p=0,01) для диастолического артериального давления.
Выводы: Безманжетное измерение артериального давления с помощью монитора электрокардиограммы с функцией фотоплетизмографии может применяться у большинства пациентов и обеспечивает надежные результаты с минимальными отличиями от значений, полученных с использованием сфигмоманометра с манжетой. Необходимо проведение дальнейших исследований с большим количеством пациентов для изучения потенциала применения метода в клинической практике.
Ключевые слова
Артериальная гипертензия (АГ) является ведущим фактором риска сердечно-сосудистой заболеваемости и смертности [1]. Точное определение артериального давления (АД) позволяет проводить своевременную диагностику и назначать соответствующее лечение АГ.
«Золотым стандартом» определения систолического и диастолического артериального давления (САД и ДАД) является прямой метод. Однако он не используется в широкой клинической практике из-за инвазивности процедуры, необходимости наличия специального оборудования и риска развития осложнений [2]. В настоящее время измерение АД с помощью приборов с использованием манжеты является методом выбора в реальной клинической практике. Методы измерения АД с использованием манжеты могут быть не совсем точными и, как правило, зависят от опыта человека, проводящего измерение, а также от индивидуальных особенностей пациента (например, наличия ожирения или отечности, частоты дыхательных движений) [3][4]. Кроме этого, использование манжеты может оказаться неудобным и вызывать дискомфорт у пациента, особенно при самостоятельном измерении АД.
Безманжетное определение АД предложено для решения некоторых из этих проблем с целью обеспечения более широкого применения в различных условиях и, следовательно, улучшения контроля давления, а также облегчения самостоятельного мониторинга АД. В настоящее время разрабатываются различные устройства для безманжетного измерения АД, большинство из которых используют фотоплетизмографию (ФПГ).
ФПГ является оптическим методом, который основан на определении изменений объема крови в артериолах от систолы к диастоле [5]. Измерение АД с помощью этого метода проводится в периферических артериолах пальцев рук. В некоторых исследованиях в качестве основного параметра для безманжетного определения АД рассматривают время прохождения пульсовой волны (ВППВ) [6] – время от зубца R на электрокардиограмме (ЭКГ) до определенной точки на ФПГ. Таким образом, для оценки ВППВ необходима одновременная регистрация ЭКГ и ФПГ [7][8][9]. Взаимосвязь между ВППВ и АД была подтверждена в некоторых исследованиях. Но большинство устройств на основе ВППВ были недостаточно удобными и не подходили для ежедневного использования [10][11].
По данным литературы, также разработаны модели для оценки АД, основанные только на характеристиках ФПГ. Однако большинство исследователей предлагали экспериментальные модели и изучали небольшие группы людей [12][13]. Таким образом, проблема разработки удобных и портативных приборов для безманжетного измерения АД остается актуальной, а их внедрение в клиническую практику требует оценки достоверности результатов измерения АД.
Одним из аппаратов для безманжетного измерения АД служит CardioQVARK® (ООО «Л Кард», Россия), представляющий собой одноканальный ЭКГ-монитор с функцией ФПГ, выполненный в виде чехла для смартфона1.
Цель исследования: оценить достоверность результатов измерения АД с помощью устройства для безманжетного определения АД (CardioQVARK®) по сравнению со значениями, полученными при измерении по методу Короткова.
МАТЕРИАЛЫ И МЕТОДЫ
Проведено обсервационное поперечное исследование, в котором сравнивались показатели АД, полученные с помощью двух подходов: безманжетного измерения на основании ФПГ (новый метод) и измерения АД с использованием сфигмоманометра с манжетой (стандартный метод). Исследование одобрено Локальным этическим комитетом (протокол № 14-19 от 13.11.2019); выполнено на базе Университетской клинической больницы №1 ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет). Осуществлялся сплошной набор пациентов, находившихся на лечении в отделении кардиологии. Сроки проведения исследования: с 01.12.2019 по 30.03.2020.
Критерии включения в исследование:
- возраст старше 18 лет;
- диагностированная АГ;
- подписанное письменное информированное согласие пациента на участие в исследовании.
Критерии невключения:
- нарушение ритма и проводимости на момент записи ЭКГ (WPW-синдром, частая желудочковая экстрасистолия; синоатриальные блокады 2-й и 3-й степени, атриовентрикулярная блокада 3-й степени, полная блокада правой или левой ножки пучка Гиса);
- состояния, ухудшающие качество записи ЭКГ (болезнь Паркинсона, эссенциальный тремор);
- установленный кардиостимулятор, кардиоресинхронизирующее устройство или кардиовертер-дефибриллятор.
Критерии исключения:
- желание прекратить участие в исследовании на любом из его этапов;
- возникновение нарушения ритма сердца в момент записи ЭКГ и пульсовой волны;
- плохое качество записи ЭКГ и пульсовой волны.
Критериям включения/невключения соответствовали 55 пациентов. В итоговый анализ включены 50 пациентов, пять исключены по разным причинам: нежелание продолжить участие в исследовании (n = 2), плохое качество записи ЭКГ и пульсовой волны (n = 2), нарушение ритма сердца в момент исследования (n = 1) (рис. 1).
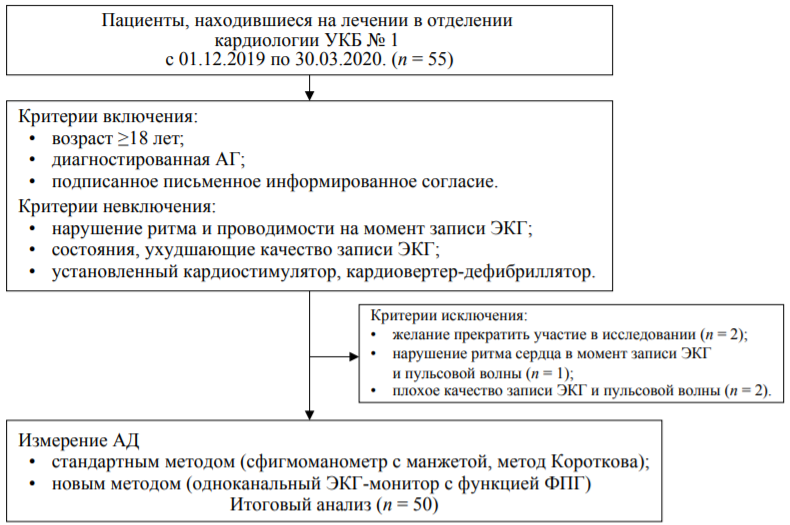
РИС. 1. Потоковая диаграмма включения пациентов в исследование
FIG. 1. Flowchart of patient inclusion in the study
АГ определяли по САД ≥ 140 мм рт. ст. или ДАД ≥ 90 мм рт. ст., а также по наличию в анамнезе диагностированной гипертонии или приема антигипертензивных препаратов [14].
Измерение артериального давления и сбор данных
Всем участникам исследования в качестве стандартного метода было выполнено измерение АД аускультативным методом (метод Короткова) с помощью сфигмоманометра с манжетой подходящего размера (Microlife BP AG1-10, Шэньчжэнь, Китай) в соответствии с рекомендациями Всемирной организации здравоохранения. Пациент спокойно сидел в течение 5 минут перед измерением, манжета накладывалась на левое плечо на 2 см выше локтя. АД определяли три раза (с интервалом в 1 минуту) и рассчитывали средние значения [15].
Не более чем через одну минуту после измерения АД стандартным методом, в положении сидя начиналась трехминутная регистрация ЭКГ и ФПГ с помощью прибора CardioQVARK® (ООО «Л Кард», Москва, Россия), предоставленного компанией-производителем. Данный прибор представляет собой персональный электрокардиограф, выполненный в виде чехла для смартфона, на который предварительно было установлено программное обеспечение. Необходимо ввести исходные данные: пол, рост и вес, далее произвести синхронную запись ЭКГ и ФПГ, результаты которых передаются на сервер, где на основании специально разработанного алгоритма с использованием обработки сигналов на основе вейвлет-преобразования рассчитывается АД. Данный алгоритм был построен с применением методов искусственного интеллекта на основании анализа большого массива данных, расчет уровня АД производится по параметрам пульсовой волны и ЭКГ (контурный анализ), а также временного интервала от R-зубца на ЭКГ до позиции определенных точек на ФПГ. Основные параметры пульсовой волны, которые используются для расчета АД, показаны на рисунке 2. Запись ЭКГ в приборе производится при помощи двух датчиков, на которые накладываются указательные пальцы рук; производится запись I стандартного отведения. Один из датчиков также проводит непрерывную запись ФПГ изображения пульсовой волны, синхронизированную с циклами ЭКГ. Способ записи ЭКГ и ФПГ представлен
на рисунке 2.
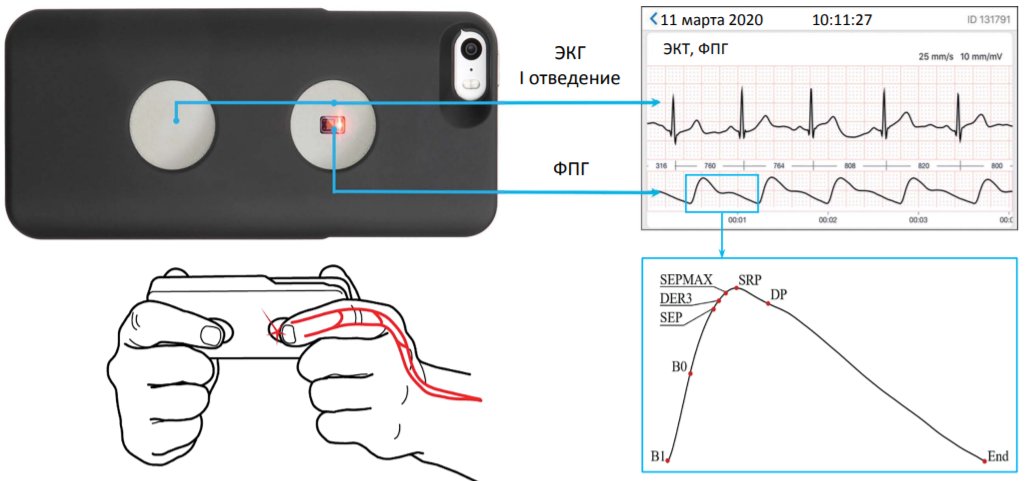
РИС. 2. Запись электрокардиограммы и фотоплетизмограммы с помощью CardioQVARK®, выполненного в виде чехла для смартфона
FIG. 2. Electrocardiogram and photoplethysmogram recording with CardioQVARK®, designed as a smartphone case
Статистическая обработка данных
Для проверки гипотез на нормальность применялись критерии Колмогорова – Смирнова и Шапиро – Уилка. Нормально распределенные непрерывные переменные были выражены как среднее ± стандартное отклонение. Проводилось сравнение показателей САД и ДАД, измеренных при помощи нового и стандартного методов. Для сравнения применялся корреляционный анализ, t-критерий Стьюдента. Вычислены коэффициенты корреляции (r), определена сила связи по шкале Чеддока. Оценка согласованности результатов измерений АД, полученных двумя разными методами, проводилась с помощью метода Блэнда – Алтмана, рассчитывались стандартное отклонение разности и его 95% доверительный интервал (95% ДИ), средняя разность между измерениями (смещение, Bias) и ее 95% ДИ. Рассчитаны чувствительность, специфичность, точность. Различия считали статистически значимыми при p < 0,05. Данные обрабатывались с помощью программы Statistica 13.0 (TIBCO, США).
РЕЗУЛЬТАТЫ
Возраст участников исследования варьировал от 33 до 85 лет, соотношение мужчины : женщины составило 1 : 1. Все 50 пациентов принимали антигипертензивные препараты, включая ингибиторы ангиотензинпревращающего фермента, блокаторы рецепторов ангиотензина, антагонисты кальция, бета-блокаторы и/или тиазидные диуретики. У 2/3 пациентов диагностирована ГБ 2-й стадии. Характеристика нашей выборки представлена в таблице 1.
Таблица 1. Основные характеристики пациентов (n = 50)
Table 1. Main characteristics of the patients (n = 50)
|
Характеристика / Feature |
Значения / Numeric values |
|
Средний возраст, лет / Average age, years |
60,0 ± 13,7 |
|
Мужчины / Men, n (%) |
25 (50%) |
|
ИМТ / BMI |
27,9 ± 5,0 |
|
Артериальная гипертензия / Arterial hypertension |
|
|
1-я стадия / 1st stage, n (%) |
12 (24%) |
|
2-я стадия / 2nd stage, n (%) |
33 (66%) |
|
3-я стадия / 3rd stage, n (%) |
5 (10%) |
|
Уровень АД выше нормы на момент исследования / Blood pressure is above normal at the time of the study, n (%) |
13 (26%) |
|
Ишемическая болезнь сердца / Ischemic heart disease, n (%) |
22 (44%) |
|
Курение ≥ 5 лет до включения в исследование / Smoking ≥ 5 years before study enrollment, n (%) |
13 (26%) |
|
Сахарный диабет 2-го типа / Type 2 diabetes mellitus, n (%) |
6 (12%) |
Note: BMI – body mass index.
Из пациентов, включенных в работу, у 14 (28%) пациентов отмечалась избыточная масса тела, у 4 (8%) – ожирение 1-й степени. Пациентов с ИМТ ниже 18,5 и выше 35 не было.
Распределение пациентов по уровню АД представлено на рисунке 3. Большинство пациентов – 34 (68%) имели уровень САД в пределах 110– 149 мм рт. ст. и 41 (82%) – показатели ДАД в пределах 60–89 мм рт. ст.
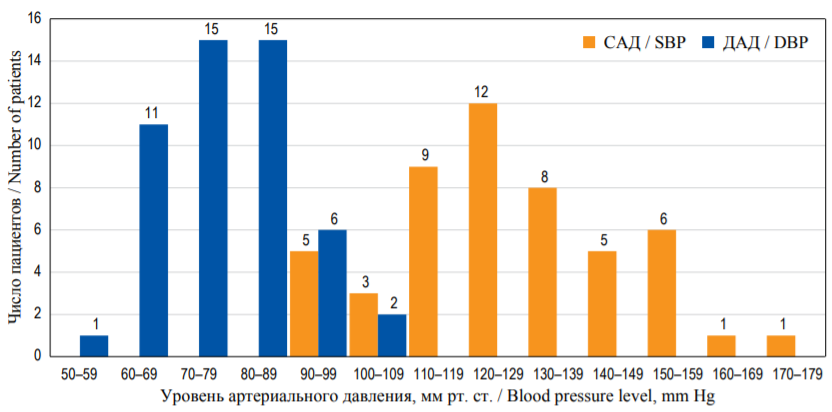
РИС. 3. Распределение пациентов по уровню систолического и диастолического артериального давления (метод Короткова)
FIG. 3. Distribution of the patients by the level of systolic and diastolic blood pressure (Korotkov method)
Среднее САД у пациентов, включенных в исследование, составило 124 ± 19 мм рт. ст. (мин – макс: 90–170 мм рт. ст.) при измерении с помощью сфигмоманометра. Среднее ДАД, измеренное с использованием манжетного тонометра, составило 75 ± 11 мм рт. ст. (мин – макс: 55–100 мм рт. ст.). При измерении монитором CardioQVARK® среднее САД и ДАД составило соответственно 125 ± 19 мм рт. ст. (мин – макс: 88–166 мм рт. ст.) и 75 ± 10 мм рт. ст. (мин – макс: 57–98 мм рт. ст.). Средние уровни САД и ДАД, стандартные отклонения, минимальные и максимальные значения для двух методов измерения АД были сопоставимы, статистически значимых различий не выявлено. Корреляционный анализ показал сильную прямую статистически значимую связь между показателями САД (r = 0,976, p < 0,0001) и ДАД (r = 0,817, p < 0,0001), измеренными двумя методами.
Метод Блэнда – Алтмана для систолического артериального давления
Нижний и верхний пределы согласованности для САД составили –8,7 мм рт. ст. (95% ДИ: –10,7; –6,6) и 7,7 мм рт. ст. (95% ДИ 5,6; 9,7) соответственно, смещение (Bias): –0,5 мм рт. ст. (95% ДИ: –1,7; 0,7) для нового метода. Данные представлены на рисунке 4а. При корреляционном анализе не отмечено значимой зависимости от уровня АД разницы измерений САД новым методом по сравнению со стандартным (рис. 4б).
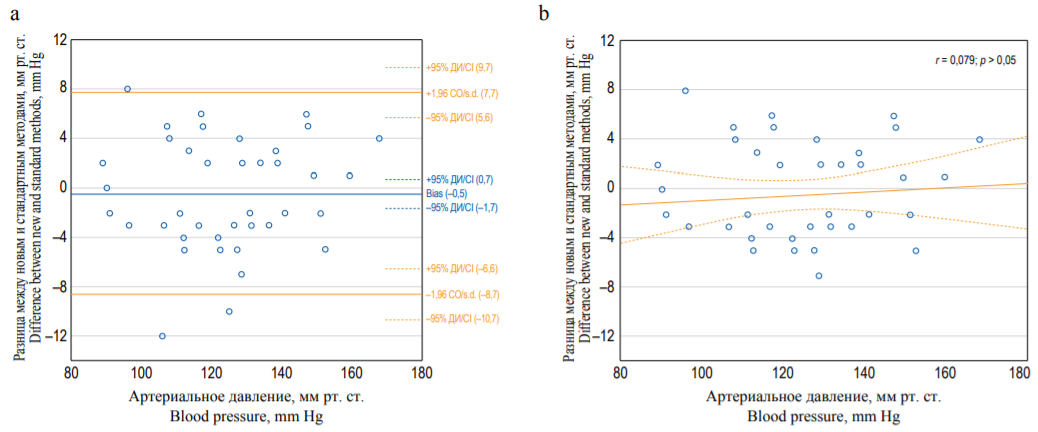
РИС. 4. Зависимость разницы значений систолического АД, измеренного методом фотоплетизмографии и аускультативным методом, от среднего значения АД: a – график Блэнда – Алтмана; Bias-смещение, 95% ДИ – 95% доверительный интервал; СО-стандартное отклонение; b – корреляция
FIG. 4. Dependence of the difference in systolic blood pressure measured by photopelysmography and auscultatory method on the mean blood pressure: a – Bland – Altman plot; Bias – 95% CI – 95% Confidence Interval; s.d. – standart deviation; b – correlation
Метод Блэнда – Алтмана для диастолического артериального давления
Для ДАД нижний предел согласованности составил –7,3 мм рт. ст. (95% ДИ: –9,1; –5,6) и верхний – 6,7 мм рт. ст. (95% ДИ: 4,9; 8,4) соответственно, смещение (Bias): –0,3 мм рт. ст. (95% ДИ: –1,4; 0,7) для нового метода. Данные представлены на рисунке 5а. При определении зависимости разницы измерений ДАД от уровня АД была выявлена значимая корреляция умеренной силы. Коэффициент корреляции составил r = 0,302 (p = 0,03). Занижение значений АД было более выражено для низких значений АД 55–75 мм рт. ст. (рис. 5б).

РИС. 5. Зависимость разницы значений диастолического АД, измеренного методом фотоплетизмографии и аускультативным методом, от среднего значения АД: a – график Блэнда – Алтмана; Bias-смещение, 95% ДИ – 95% доверительный интервал; СО – стандартное отклонение; b – корреляция
FIG. 5. Dependence of the difference in diastolic blood pressure measured by photopelysmography and auscultatory method on the mean blood pressure: a – Bland – Altman plot; Bias – 95% CI – 95% Confidence Interval; s.d. – standart deviation; b – correlation
На момент проведения исследования у 13 (26%) пациентов отмечалось повышение АД (табл. 1). Чувствительность нового метода в выявлении АГ составила 77% (95% ДИ 46; 95), специфичность 100% (95% ДИ 91; 100), точность 94% (95% ДИ 83; 99).
ОБСУЖДЕНИЕ
Результаты этого пилотного валидационного исследования для CardioQVARK® демонстрируют хорошую корреляцию между измерениями САД и ДАД, полученными с помощью ФПГ и стандартным методом с помощью тонов Короткова. Это указывает на то, что инфракрасный свет, используемый при ФПГ, имеет достаточную глубину проникновения для исследования периферических артериол и оценки артериального давления с помощью сигналов пульсовой волны, что делает возможным применение безманжетного измерения АД [16][17]. При проведении анализа Блэнда – Алтмана смещение для значений САД и ДАД составило 0,5 мм рт. ст. и менее в сторону занижения.
В 2017 году проводилось исследование, в котором сравнивались результаты измерений АД, проводимые в течение 24 часов с помощью прибора Somnotouch-NIBP (Somnomedics GmbH, Randersacker, Германия) и осциллометрического тонометра [18]. Устройство Somnotouch-NIBP определяет АД на основе времени прохождения пульсовой волны, которое регистрируется с помощью датчика ФПГ и электродов ЭКГ. Среднее абсолютное расхождение для САД и ДАД составило 10,2 и 8,2 мм рт. ст. Таким образом, среднее расхождение для САД и ДАД было больше, чем в нашем исследовании. Кроме того, прибор регистрирует несколько отведений ЭКГ и требует использования соответствующего специального оборудования (т.е. является неудобным в повседневном применении). Коэффициенты корреляции составили для САД 0,88, для ДАД 0,85. В нашем исследовании получен больший коэффициент корреляции для САД (0,98) и близкий к упомянутому выше исследованию для ДАД (0,82).
В 2019 году было опубликовано исследование портативного прибора для измерения артериального давления (Model T2; TMART Technologies Limited, Гонконг, Китай) [19]. Данный прибор носится на запястье и имеет встроенный датчик движения MPU6500, с помощью которого проводится измерение АД. Одной из задач исследования было сравнить значения АД, измеренные портативным прибором, с цифрами АД, зарегистрированными с помощью автоматического осциллометрического тонометра с использованием манжеты. Измерения проводились в течение 7 дней. Среднее смещение составило для САД –12,7 мм рт. ст. (95% ДИ: –28,7; –3,4) и для ДАД –5,6 мм рт. ст. (95% ДИ: –20,5; –9,2). В рамках данной работы также производилось сравнение измерения АД с помощью портативного прибора с устройством для суточного мониторирования АД в течение 24 часов, которое показало среднее смещение для САД 0,5 (–10,1; 11,1) мм рт. ст. и для ДАД 2,24 (–17,6; 13,1) мм рт. ст. Несмотря на то что устройство продемонстрировало довольно неплохие результаты при суточном мониторировании АД, измерения в течение 7 дней значительно отличались от референсных значений. Среднее расхождение цифр АД, зарегистрированных прибором Model T2 (TMART Technologies Limited) при измерении АД в течение как 24 часов, так и 7 дней, было выше в сравнении с нашей работой.
Из включенных в наше исследование пациентов у двоих было выявлено плохое качество записи ЭКГ и пульсовой волны, однако определить причину низкого качества записи или закономерность, характерную для этих пациентов, не удалось.
Измерение АД с помощью манжеты вызывает определенные трудности у некоторых пациентов [20], например при ожирении трудно подобрать подходящий размер манжеты. Кроме того, сфигмоманометры необходимо регулярно проверять и калибровать. Ряд этих неудобств препятствует широкому применению самостоятельного мониторинга АД, а также затрудняет использование в рамках телемедицины.
Использование безманжетного определения АД имеет большой потенциал для упрощения и облегчения самостоятельного измерения АД для многих пациентов. Тот факт, что к коммерчески доступному смартфону легко подключить специальный монитор, выполненный в виде чехла для телефона, является преимуществом, обеспечивающим бóльшую независимость и удобство для пациентов, а также контроль за состоянием их здоровья. Возможность измерять АД в любое время и любом месте является еще одним преимуществом. Измерение АД в домашних условиях может быть более эффективным, чем измерение в медицинском учреждении, что связано с исключением гипертонии «белого халата». Передача результатов домашних измерений с помощью телемедицинских технологий может также облегчить подбор лекарственных средств и их оптимальных дозировок, что в итоге может способствовать снижению заболеваемости и смертности у пациентов с АГ [21].
Ограничения исследования и направления для дальнейших исследований
Количество участников данного исследования было относительно небольшим. Поэтому, чтобы лучше определить точность и надежность метода, необходимо проведение дальнейших исследований. Также стоит изучить влияние помех на точность метода определения АД с использованием модели машинного обучения [22][23][24]. Это довольно важный момент, поскольку безманжетное определение АД зависит от качества записи ФПГ. В данной работе регистрация ЭКГ и ФПГ проводилась с пальцев рук, однако не учитывались особенности кровенаполнения пальцев (объем пальца, влажность, температура), для изучения данного вопроса необходимо проведение более расширенных исследований. Еще одним недостатком этого исследования является использование только неинвазивных методов в качестве контрольных измерений АД. Кроме того, распределение пациентов по уровню АД было не совсем равномерным, практически отсутствовали пациенты с низкими и высокими цифрами АД. Также в исследовании не было пациентов с ожирением 2-й, 3-й степени и с дефицитом веса. Равномерное распределение по уровню давления, значению ИМТ и другим клиническим показателям могло бы лучше отразить точность измерения АД с помощью рассматриваемого метода. Несмотря на то что в этом исследовании была подтверждена возможность использования пульсовой волны для безманжетного определения АД, для более широкого применения этого метода необходимо дальнейшее изучение влияния различных факторов (индивидуальных, внешних) на качество записи ЭКГ и пульсовой волны, а также проведение более крупных исследований с бóльшим количеством участников.
ВЫВОДЫ
Метод измерения АД на основе анализа ЭКГ и ФПГ с помощью прибора CardioQVARK® продемонстрировал достоверные результаты измерения АД по сравнению с методом Короткова: выявлена статистически значимая корреляция для САД (r = 0,976) и ДАД (r = 0,817), по данным анализа Блэнда – Алтмана смещение составило –0,5 и –0,3 мм рт. ст. для САД и ДАД соответственно. Чувствительность нового метода в выявлении АГ составила 77% (95% ДИ 46; 95), специфичность 100% (95% ДИ 91; 100), точность 94% (95% ДИ 83; 99).
ВКЛАД АВТОРОВ
Ф.Ю. Копылов, Х. Санер, П.Ш. Чомахидзе внесли основной вклад в разработку концепции статьи и дизайна исследования. П.Ш. Чомахидзе, Д.Г. Гогниева участвовали в сборе данных и подготовке материалов для публикации, провели статистический анализ. Н.А. Гогиберидзе, Н.О. Кузнецова, Ж.Н. Сагирова внесли существенный вклад в написание статьи. Все авторы утвердили окончательную версию статьи.
AUTHOR CONTRIBUTIONS
Philipp Yu. Kopylov, Hugo Saner, Petr Sh. Chomakhidze made the major contribution to the development of the concept of the article and design of the study. Petr Sh. Chomakhidze, Daria G. Gognieva participated in the collection and interpretation of the data, conducted statistical analysis of the data. Nana A. Gogiberidze, Natalia O. Kuznetsova, Zhanna N. Sagirova made a significant contribution to the writing of the article. All authors approved the final version of the publication.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Исследование не имело спонсорской поддержки (собственные ресурсы).
Conflict of interests. The authors declare that there is no conflict of interests.
Financial support. The study was not sponsored (own resources).
Список литературы
1. Whelton P.K., Carey R.M. The 2017 Clinical Practice Guideline for High Blood Pressure. JAMA. 2017; 318(21): 2073–2074. https://doi.org/10.1001/jama.2017.18209 PMID: 29159375
2. McEniery C.M., Cockcroft J.R., Roman M.J., et al. Central blood pressure: current evidence and clinical importance. Eur Heart J. 2014; 35(26): 1719–1725. https://doi.org/10.1093/eurheartj/eht565 PMID: 24459197
3. Van Montfrans G.A. Oscillometric blood pressure measurement: progress and problems. Blood Pressure Monitoring. 2001; 6(6): 287–290. https://doi.org/10.1097/00126097-200112000-00004 PMID: 12055403
4. Zheng D., Di Marco L.Y., Murray A. Effect of respiration on Korotkoff sounds and oscillometric cuff pressure pulses during blood pressure measurement. Med Biol Eng Comput. 2014; 52(5): 467–473. https://doi.org/10.1007/s11517-014-1150-1 PMID: 24668326
5. Xing X., Sun M. Optical blood pressure estimation with photoplethysmography and FFT-based neural networks. Biomed Opt Express 2016; 7(8): 3007–3020. https://doi.org/10.1364/BOE.7.003007 PMID: 27570693
6. Yoon Y., Cho J.H., Yoon G. Non-constrained blood pressure monitoring using ECG and PPG for personal Healthcare. J Med Syst. 2009; 33(4): 261–266. https://doi.org/10.1007/s10916-008-9186-0 PMID: 19697692
7. Lin W.H., Wang H., Samuel O.W., et al. New photoplethysmogram indicators for improving cuffless and continuous blood pressure estimation accuracy. Physiol. Meas. 2018; 39(2): 025005. https://doi.org/10.1088/1361-6579/aaa454 PMID: 29319536
8. Ding X.R., Zhang Y.T., Liu J., et al. Continuous cufless blood pressure estimation using pulse transit time and photoplethysmogram intensity ratio. IEEE Trans Biomed Eng. 2016; 63(5): 964–972. https://doi.org/10.1109/TBME.2015.2480679 PMID: 26415147
9. Gao M., Olivier N.B., Mukkamala R. Comparison of noninvasive pulse transit time estimates as markers of blood pressure using invasive pulse transit time measurements as a reference. Physiological Rep. 2016; 4(10): e12768. https://doi.org/10.14814/phy2.12768 PMID: 27233300
10. Tang Z., Sekine M., Tamura T., et al. A chair for cuffless real-time estimation of systolic blood pressure based on pulse transit time. Annu Int Conf IEEE Eng Med Biol Soc. 2015; 2015: 5118–5121. https://doi.org/10.1109/EMBC.2015.7319543 PMID: 26737443
11. Mukkamala R., Hahn J.O., Inan O.T., et al. Toward ubiquitous blood pressure monitoring via pulse transit time: theory and practice. IEEE Trans Biomed Eng. 2015; 62(8):1879–1901. https://doi.org/10.1109/TBME.2015.2441951 PMID: 26057530
12. Fukushima H., Kawanaka H., Bhuiyan M.S., Oguri K. Cuffless blood pressure estimation using only photoplethysmography based on cardiovascular parameters. Annu Int Conf IEEE Eng Med Biol Soc. 2013; 2013: 2132–2135. https://doi.org/10.1109/EMBC.2013.6609955 PMID: 24110142
13. Shimazaki S., Bhuiyan S., Kawanaka H., Oguri K. Features extraction for cuffless blood pressure estimation by autoencoder from photoplethysmography. Annu Int Conf IEEE Eng Med Biol Soc. 2018 Jul; 2018: 2857–2860. https://doi.org/10.1109/EMBC.2018.8512829 PMID: 30440997
14. Williams B., Mancia G., Spiering W., et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology (ESC) and the European Society of Hypertension (ESH). Eur Heart J. 2018; 39(33): 3021–3104. https://doi.org/10.1093/eurheartj/ehy339 PMID: 30165516
15. Whitworth J.A., World Health Organization, International Society of Hypertension Writing Group. 2003 World Health Organization (WHO)/International Society of Hypertension (ISH) statement on management of hypertension. J Hypertens. 2003; 21(11):1983–1992. https://doi.org/10.1097/00004872-200311000-00002 PMID: 14597836
16. Peng X., Schultz M.G., Picone D.S., et al. Non-invasive measurement of reservoir pressure parameters from brachial-cuff blood pressure waveforms. J Clin Hypertens (Greenwich) 2018; 20(12): 1703–1711. https://doi.org/10.1111/jch.13411 PMID: 30450732
17. Matsumura K., Rolfe P., Toda S., Yamakoshi T. Cuffless blood pressure estimation using only a smartphone. Sci Rep. 2018; 8(1): 7298. https://doi.org/10.1038/s41598-018-25681-5 PMID: 29740088
18. Krisai P., Vischer A.S., Kilian L., et al. Accuracy of 24-hour ambulatory blood pressure monitoring by a novel cuffless device in clinical practice. Heart. 2019; 105(5): 399–405. https://doi.org/10.1136/heartjnl-2018-313592 PMID: 30228251
19. Islam S.M.S., Cartledge S., Karmakar C., et al. Validation and acceptability of a cuffless wrist-worn wearable blood pressure monitoring device among users and health care professionals: mixed methods study. JMIR Mhealth Uhealth. 2019; 7(10): e14706. https://doi.org/10.2196/14706 PMID: 31628788
20. Liu Z.D., Liu J.K., Wen B., et al. Cuffless blood pressure estimation using pressure pulse wave signals. Sensors. 2018; 18(12): 4227. https://doi.org/10.3390/s18124227 PMID: 30513838
21. Bard D.M., Joseph J.I., van Helmond N. Cuff-Less methods for blood pressure telemonitoring. Front Cardiovasc Med. 2019; 6: 40. https://doi.org/10.3389/fcvm.2019.00040 PMID: 31157236
22. Khalid S.G., Zhang J., Chen F., Zheng D. Blood pressure estimation using photoplethysmography only: comparison between different machine learning approaches. J Healthc Eng. 2018 Oct 23; 2018: 1548647. https://doi.org/10.1155/2018/1548647 PMID: 30425819
23. Eom H., Lee D., Han S., et al. End-to-End deep learning architecture for continuous blood pressure estimation using attention mechanism. Sensors. 2020; 20(8): 2338. https://doi.org/10.3390/s20082338 PMID: 32325970
24. Liu Z., Miao F. Wang R., et al. Cuff-less blood pressure measurement based on deep convolutional neural network. Annu Int Conf IEEE Eng Med Biol Soc. 2019 Jul; 2019: 3775–3778. https://doi.org/10.1109/EMBC.2019.8856588 PMID: 31946696
Об авторах
Н. А. ГогиберидзеРоссия
Гогиберидзе Нана Автандиловна, ассистент кафедры кардиологии, функциональной и ультразвуковой диагностики
ул. Трубецкая, д. 8, стр. 2, г. Москва, 119991
Ж. Н. Сагирова
Россия
Сагирова Жанна Насибуллаевна, аспирант кафедры кардиологии, функциональной и ультразвуковой диагностики
ул. Трубецкая, д. 8, стр. 2, г. Москва, 119991
Н. О. Кузнецова
Россия
Кузнецова Наталья Олеговна, аспирант кафедры кардиологии, функциональной и ультразвуковой диагностики
ул. Трубецкая, д. 8, стр. 2, г. Москва, 119991
Д. Г. Гогниева
Россия
Гогниева Дарья Геннадиевна, ассистент кафедры кардиологии, функциональной и ультразвуковой диагностики
ул. Трубецкая, д. 8, стр. 2, г. Москва, 119991
П. Ш. Чомахидзе
Россия
Чомахидзе Петр Шалвович, д-р мед. наук, профессор кафедры кардиологии, функциональной и ультразвуковой диагностики
ул. Трубецкая, д. 8, стр. 2, г. Москва, 119991
Х. Санер
Швейцария
Хьюго Санер, д-р мед. наук, научный сотрудник Центра исследований в области биомедицинской инженерии; консультант
50, Берн, 3008; 18, Берн, 3010
Ф. Ю. Копылов
Россия
Копылов Филипп Юрьевич, д-р мед. наук, профессор кафедры кардиологии, функциональной и ультразвуковой диагностики
ул. Трубецкая, д. 8, стр. 2, г. Москва, 119991
Дополнительные файлы
Рецензия
JATS XML